|
文章分類 文章分類 副標(biāo)題 |
藥品穩(wěn)定性試驗箱驗證方案 二維碼
1692
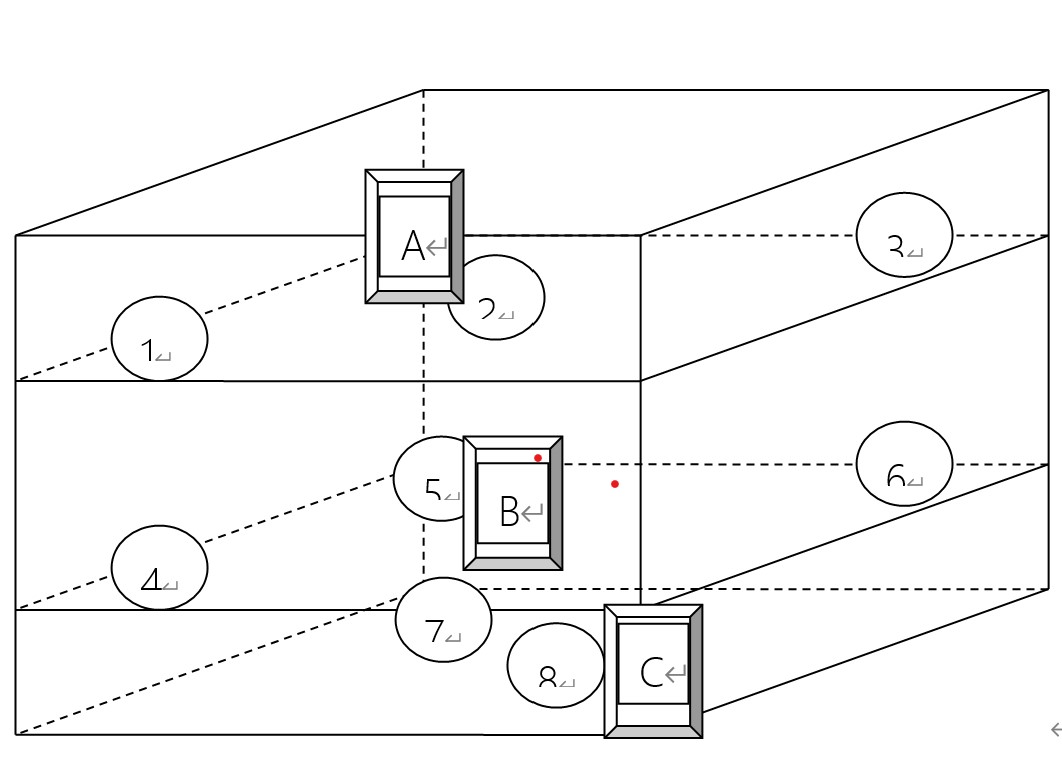
藥品穩(wěn)定性試驗箱驗證方案 編 號: 頁 碼: 共15頁,第 1頁 藥品穩(wěn)定性試驗箱驗證方案 目 錄 1.概述……………………………………………………………………………3 2.驗證目的………………………………………………………………………………3 3.驗證范圍………………………………………………………………………………3 4.驗證時間………………………………………………………………………………3 5.職責(zé)……………………………………………………………………………………3 6.相關(guān)文件………………………………………………………………………………4 7.驗證內(nèi)容及方法………………………………………………………………………4 7.1安裝確認(rèn)……………………………………………………………………4 7.2運行確認(rèn)……………………………………………………………………5 7.3性能確認(rèn)……………………………………………………………………7 8.驗證結(jié)論………………………………………………………………………8 9.再驗證周期確認(rèn)………………………………………………………………9 10.人員培訓(xùn)………………………………………………………………………9 11.偏差處理………………………………………………………………………9 12.評價與建議…………………………………………………………………9 13.附件…………………………………………………………………………9 1 概述: 正合藥品穩(wěn)定試驗箱采用鎳鉻絲電加熱器作為加熱器、二套進(jìn)口丹佛斯小型風(fēng)冷全封閉耐熱型制冷壓縮機(jī)作為制冷機(jī)調(diào)節(jié)溫度,采用電熱蒸氣式加濕器(選用純凈水或蒸餾水供水)調(diào)節(jié)設(shè)備的濕度。能提供15℃~65℃的溫度控制范圍及20%RH~95%RH的濕度控制范圍。藥品穩(wěn)定試驗箱有效空間內(nèi)各點的溫度變差應(yīng)小于設(shè)定溫度值的±2℃,溫度波動度應(yīng)小于±0.5℃,濕度變差應(yīng)小于設(shè)定濕度值的±5%RH。 2 驗證目的: 本方案用于確認(rèn)藥品穩(wěn)定性試驗箱的安裝、運行和性能確認(rèn),確保藥品穩(wěn)定性試驗箱的安裝正確,且藥品穩(wěn)定性試驗箱在合格的安裝條件下能正常運轉(zhuǎn),能提供穩(wěn)定的溫濕度條件。 3 驗證范圍: 該方案適用于藥品穩(wěn)定性試驗箱的安裝確認(rèn)、運行確認(rèn)和性能確認(rèn)。 4 驗證時間: 本次驗證計劃于 年___月___日開始實施。 5 職責(zé): 公司驗證委員會根據(jù)驗證項目,組建驗證小組,明確職責(zé),并對方案及報告進(jìn)行審批。 5.1 驗證小組組成及職責(zé): 組長: 驗證小組成員: 5.1.1 負(fù)責(zé)起草驗證方案,并組織實施。 5.1.2 負(fù)責(zé)所有的變更和偏差的批準(zhǔn)。 5.1.3 驗證完成后收集驗證記錄,審核驗證數(shù)據(jù),并起草驗證報告。 5.1.4 負(fù)責(zé)驗證的協(xié)調(diào)工作,以保證本驗證方案規(guī)定項目的順利實施。 5.1.5 確定再驗證周期。 5.1.6 負(fù)責(zé)驗證數(shù)據(jù)及結(jié)果的審核。 5.1.7 負(fù)責(zé)驗證報告的審批。 5.2 質(zhì)管部職責(zé): 5.2.1負(fù)責(zé)驗證方案和報告的審核。 5.2.2負(fù)責(zé)驗證工作的檢查與監(jiān)督,確保驗證項目正確有效實施。 5.2.3負(fù)責(zé)驗證實施中的取樣及檢驗。 5.2.4負(fù)責(zé)儀器、儀表的校驗。 本方案依據(jù)下面列出規(guī)范的有關(guān)條款,結(jié)合本公司需求制定。以下規(guī)范為有效的最新文本,設(shè)備所提供的性能及參數(shù)應(yīng)能滿足以下規(guī)范的有關(guān)要求。 A. 《化學(xué)藥物穩(wěn)定性研究技術(shù)指導(dǎo)原則》 B.《蘇州正合測試設(shè)備有限公司藥品穩(wěn)定性試驗箱ZHH-250/500SD使用說明書》 C.JJF1101- 《環(huán)境試驗設(shè)備溫度、濕度校準(zhǔn)規(guī)范》 7 驗證內(nèi)容及方法 7.1安裝確認(rèn)(IQ): 藥品穩(wěn)定性試驗箱(型號: ;編號: ),安裝于 。對藥品穩(wěn)定性試驗箱供應(yīng)商所提供的技術(shù)資料進(jìn)行核查、對藥品穩(wěn)定性試驗箱及備品備件及安裝進(jìn)行檢查。 確認(rèn)方法:開箱,對照裝箱單、備件清單、合同進(jìn)行檢查,檢查供應(yīng)商提供的圖紙、設(shè)備清單、各類證書、說明書等是否準(zhǔn)確、完整;按照供應(yīng)商提供的備品備件清單檢查實物,將清單編號存檔,將實物驗收入庫。在安裝確認(rèn)的過程中如發(fā)現(xiàn)供貨商提供的資料有差錯貨不完整,應(yīng)及時向供貨商索取。將檢查結(jié)果記錄于附錄一,并對檢查結(jié)果進(jìn)行確認(rèn)。 7.2運行確認(rèn)(OQ): 7.2.1儀器校準(zhǔn)確認(rèn) 由有資質(zhì)的檢定機(jī)構(gòu)或人員對藥品穩(wěn)定性試驗箱本體儀表及驗證儀配套儀表的校準(zhǔn)進(jìn)行檢查確認(rèn),并將檢查結(jié)果記錄填寫于附錄三。 7.2.2最低水位確認(rèn) 以潛水泵體的進(jìn)水口為最低水位,并在循環(huán)水箱箱體上標(biāo)注最低水位線。 7.2.3參數(shù)確認(rèn) 采用VaIte多路溫度驗證系統(tǒng),經(jīng)過測試藥品穩(wěn)定性試驗箱腔室內(nèi)不同點的溫度值,來證明該設(shè)備的溫、濕度準(zhǔn)確性。取8個測試點(每點放兩個探頭)如圖。
將16支檢定合格的多路溫度驗證系統(tǒng)探頭經(jīng)過測試孔分布到各點,同時將A、B、C三塊濕度計分別放在上層左后方、中層中間以及下層右前方。接通電源,將藥品穩(wěn)定性試驗箱溫濕度設(shè)定為 ℃/ %RH。 在藥品穩(wěn)定性試驗箱穩(wěn)定工作2小時后,觀察藥品穩(wěn)定性試驗箱本體儀表的溫濕度值與多路溫度驗證系統(tǒng)的溫度探頭所示的溫度平均值和三塊濕度計的濕度平均值是否一致。如有差異,調(diào)整參數(shù)Sc1和Sc3進(jìn)行校正,使其一致,并將結(jié)果記錄于附錄二。 7.2.4啟閉確認(rèn) 藥品穩(wěn)定性試驗箱從室溫開始運行到穩(wěn)定工作所需要的最少時間為啟閉時間。記錄溫度從室溫到設(shè)定溫度所用的時間,并將結(jié)果記錄于附錄二。 7.2.5開關(guān)門確認(rèn) 藥品穩(wěn)定性試驗箱穩(wěn)定工作后,打開箱門2min,然后關(guān)閉箱門,觀察箱體內(nèi)的溫濕度變化。重復(fù)操作3次,參照多路溫度驗證系統(tǒng)的運行記錄,計算開關(guān)門后藥品穩(wěn)定性試驗箱恢復(fù)穩(wěn)定工作(溫度在設(shè)定溫度的±2℃,濕度在設(shè)定濕度的±5%RH,且兩者同時滿足)所需時間,結(jié)果記錄于附錄二。 7.2.6準(zhǔn)確性測試 藥品穩(wěn)定性試驗箱連續(xù)測試4小時,參照多路溫度驗證系統(tǒng)的運行記錄和三塊濕度計的記錄數(shù)據(jù) (剔除3次開關(guān)門數(shù)據(jù)),計算出平均溫度和平均濕度。將檢查結(jié)果記錄于附錄四、五,并對檢查結(jié)果進(jìn)行確認(rèn)。 可接受標(biāo)準(zhǔn): 藥品穩(wěn)定性試驗箱顯示溫度與多路溫度驗證系統(tǒng)測試平均溫度差值不得過±1℃;藥品穩(wěn)定性試驗箱顯示濕度與測試平均濕度差值不得過±5%RH。 確認(rèn)結(jié)果: 驗證小組根據(jù)檢查的結(jié)果,同時對其進(jìn)行結(jié)果確認(rèn),并簽名。 7.2.7停電保溫性能確認(rèn) 將藥品穩(wěn)定性試驗箱溫濕度設(shè)定為 ℃/ %RH和 ℃/ %RH兩種條件下的試驗。當(dāng)藥品穩(wěn)定性試驗箱穩(wěn)定工作后,關(guān)掉藥品穩(wěn)定性試驗箱電源,記錄斷電動作時間。參照多路溫度驗證系統(tǒng)的運行記錄,計算藥品穩(wěn)定性試驗箱從停電時刻到超過設(shè)定溫度的±2℃或設(shè)定濕度的±5%RH的時間,結(jié)果記錄于附錄二。 7.3 性能確認(rèn)(PQ): 采用VaIte多路溫度驗證系統(tǒng),經(jīng)過測試恒溫恒濕箱腔室內(nèi)不同點的溫度值,來證明該設(shè)備的溫度均勻性及準(zhǔn)確性。取8個測試點(每點放兩個探頭)如圖。
將16支檢定合格的多路溫度驗證系統(tǒng)探頭經(jīng)過測試孔分布到各點,同時將A、B、C三塊濕度計分別放在上層左后方、中層中間以及下層右前方。接通電源,將藥品穩(wěn)定性試驗箱溫濕度設(shè)定為 ℃/ %RH和 ℃/ %RH兩種條件下的試驗。 分空載只做 ℃/ %RH和滿載(注:包裝物為日常待檢樣品)做 ℃/ %RH和 ℃/ %RH兩種裝載方式連續(xù)測試,各測試24小時。參照多路溫度驗證系統(tǒng)的運行記錄和三塊濕度計的記錄數(shù)據(jù),計算溫濕度變差和溫度波動度。計算公式如下: 1.溫度波動度的計算公式:△ T =±(T -T )/2 式中:△T ----溫度波動度,℃; T ----中心點n次測量中的最高溫度,℃; T ----中心點n次測量中的最低溫度,℃; 2.溫度變差的計算公式:△T = T - T 式中:△T -----溫度變差,℃; T -----中心點n次測量的平均值,℃; T ---設(shè)備顯示溫度平均值,℃; 3. 濕度變差的計算公式:△H = H - H 式中:△H ---濕度變差,%RH; H ---中心點n次測量的平均值,%RH; H ---設(shè)備顯示濕度平均值,%RH; 可接受標(biāo)準(zhǔn): 藥品穩(wěn)定性試驗箱有效空間內(nèi)各點的溫度變差應(yīng)小于設(shè)定溫度值的±2℃,溫度波動度應(yīng)小于±0.5℃,濕度變差應(yīng)小于設(shè)定濕度值的±5%RH。結(jié)果記錄于附表四、五。 確認(rèn)結(jié)果: 驗證小組根據(jù)檢查的結(jié)果,由質(zhì)管部、設(shè)備部、QC化驗室等部門對其進(jìn)行結(jié)果確認(rèn),并簽名。 8. 驗證結(jié)論 對驗證數(shù)據(jù)進(jìn)行分析,驗證總結(jié)。 9. 再驗證周期 由驗證小組根據(jù)驗證結(jié)果確定再驗證周期。 10. 人員培訓(xùn) 由驗證小組長對參加驗證的人員進(jìn)行本驗證方案的培訓(xùn),確保整個驗證過程嚴(yán)格按方案進(jìn)行。結(jié)果記錄于附錄六。 11. 偏差處理 在驗證過程中,發(fā)現(xiàn)任何偏差需按照偏差規(guī)程進(jìn)行相應(yīng)的調(diào)查及處理,并記錄。 12. 評價與建議 對驗證結(jié)果進(jìn)行評價,包括以下內(nèi)容: ① 驗證是否有遺漏? ② 驗證實施過程中對驗證方案有無修改?修改原因,依據(jù)是否經(jīng)過批準(zhǔn)? ③ 驗證記錄是否完整? ④ 驗證試驗結(jié)果是否符合要求?對偏差的處理是否合理?是否需要進(jìn)一步補充試驗? ⑤ 經(jīng)過本次驗證,對本儀器的使用有何建議? 13. 附件 附錄一 藥品穩(wěn)定性試驗箱安裝確認(rèn)項目檢查表 附錄二 藥品穩(wěn)定性試驗箱運行確認(rèn)項目檢查表 附錄三 儀表檢定確認(rèn)表 附錄四 濕度原始數(shù)據(jù) 附錄五 溫濕度波動度及偏差結(jié)果 附錄六 驗證小組培訓(xùn)記錄 附錄一 藥品穩(wěn)定性試驗箱安裝確認(rèn)項目檢查表
附錄二 藥品穩(wěn)定性試驗箱運行確認(rèn)項目檢查表
附錄三 儀表檢定確認(rèn)表
附錄四 濕度原始數(shù)據(jù)
附錄五 溫濕度波動度及偏差結(jié)果
附錄六 驗證小組培訓(xùn)記錄
|
||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
文章列表
副標(biāo)題